Nội dung chính
Case bệnh: Bệnh nhân nữ 39 tuổi bị đánh trống ngực, đau bụng và nôn ói – tải PDF Tại đây.
Biên dịch: Bs Hoàng Nam
Bệnh cảnh lâm sàng
Bác sĩ Kelsey Hills-Evans: Bệnh nhân nữ 39 tuổi bị hội chứng nôn chu kỳ và rối loạn đa chất gây nghiện nhập khoa cấp cứu bệnh viện Massachusetts trong tình trạng đau bụng và nôn nói.
Cách nhập viện 11 tuần, bệnh nhân nhập bệnh viện địa phương vì buồn nôn và nôn ói khó kiểm soát. Bệnh kèm theo tiêu phân lỏng vả đau hố chậu phải khi có kinh nguyệt. Các triệu chứng tương tự lần nhập viện trước được cho do hội chứng nôn ói chu kỳ. Xét nghiệm độc tố Clostridium và tìm bạch cầu trong phân đều âm tính, xét nghiệm phân để tìm trứng và ký sinh trùng cũng âm tính, cấy phân cho thấy hệ vi khuẩn đường ruột bình thường. Xét nghiệm độc chất trong nước tiểu phát hiện dương tính với cocaine và thuốc phiện. Làm thêm các cận lâm sàng hình ảnh học.
Bác sĩ Mark A. Anderson: Chụp cắt lớp vi tính (CTscan) ổ bụng và vùng chậu sau khi tiêm tĩnh mạch thuốc cản quang, phát hiện sỏi thận 2 bên nhỏ, không gây tắc nghẽn, thận không ứ nước. Không có bằng chứng tắc ruột hoặc tình trạng viêm cấp tính vùng bụng và chậu, kể cả viêm ruột thừa. Buồng trứng tiền mãn kinh bình thường, chứa các nang chức năng.
Bác sĩ Hills-Evans: dùng thuốc ondasetron (thuốc chống nôn), hydromorphone (thuốc giảm đau gây nghiện) và các dịch truyền. Bệnh nhân giảm buồn nôn, nôn ói và đau bụng. Ngày thứ 2 nhập viện, bệnh nhân có thể ăn bình thường và xuất viện về nhà.
Cách nhập viện 1 ngày, bệnh nhân hít phải khói do chập điện trong tầng hầm. Sau khi hít phải khói đó, bệnh nhân thấy đau hố chậu trái và mệt mỏi dữ dội, nhưng không đi khám. Cùng ngày nhập viện, khi bắt đầu chu kỳ kinh nguyệt, bệnh nhân thức dậy trong tình trạng buồn nôn và nôn ra nhiều dịch nâu sẫm. Bệnh nhân tự đo nhiệt độ tại nhà là 39.4 độ C. Trong 12 giờ tiếp theo, bệnh nhân buồn nôn dai dẳng và nôn ói nhiều lần. Bệnh nhân thấy ngày càng yếu, choáng váng và chóng mặt nên nhập khoa cấp cứu bệnh viện Massachusetts để khám.
Tại khoa cấp cứu, bệnh nhân vẫn buồn nôn, nôn ói và đau hố chậu trái. Gần đây bệnh nhân có sử dụng chất tổng hợp cannabinoids, không dùng các thuốc khác. Tiền sử bệnh gồm sỏi thận, hen suyễn, viêm mũi dị ứng, đau lưng mạn tính, trầm cảm, trào ngược dạ dày thực quản và đau bụng kinh nặng. Tiền sữ phẫu thuật gồm thay khớp vai, thu nhỏ tuyến vú và cắt nang buồng trứng. Tiền sử dùng thuốc gồm acetaminophen, fluticasone nhỏ mũi, fluticasone propionate dạng xịt, albuterol, promethazine, ondansetron, polyethylene glycol và multivitamin. Bệnh nhân không dị ứng với thức ăn và thuốc. Không rõ tiền sử bệnh trong gia đình. Cách đây 3 năm, bệnh nhân có đến sống ở New England từ vùng Tây Bắc Hoa Kỳ sau khi lấy chồng. Bệnh nhân làm trong ngành dược nhưng đã nghỉ việc cách đây 3 tháng vì hội chứng nôn ói chu kỳ. Bệnh nhân không hút thuốc lá và không uống rượu. Bệnh nhân có dùng cocaine, heroin, cần sa và 3,4-methylenedioxymethamphetamine (MADA).
Sinh hiệu: nhiệt độ 37.2 độ C, mạch 165 lần/phút, huyết áp 152/70 mmHg, nhịp thở 22 lần/phút, Sp02 = 100% (khí trời). Cân nặng hiện tại 52.5 kg; cách nhập viện 11 tuần, bệnh nhân nặng 59.3 kg. Bệnh nhân tỉnh, định hướng tốt nhưng không ổn định, ghi nhận các lần cười và khóc xen lẫn nhau. Ánh nhìn dữ tợn, nói nhanh, hấp tấp và đôi khi nói ngọng nghịu. Bệnh nhân dễ kích động và lúc khám thấy đang quẫy đạp trên giường. Mặt và ngực nổi ban đỏ, sờ vào da thì ấm. Tay run nhẹ, khám không thấy giật lưỡi. Bệnh nhân không hợp tác khi khám cổ. Tim nhanh và đều; ghi nhận âm thổi tâm thu lúc tống máu. Bụng mềm, nhu động ruột bình thường, không chướng. Ấn đau hố chậu trái.
Ngay sau khi nhập khoa cấp cứu, bệnh nhân nôn ra dịch “bã cà phê”. Khoảng 25 phút sau, mạch tăng lên 165 – 210 lần/phút.
Bác sĩ D. Barrett: Điện tâm đồ 12 chuyển đạo tại khoa cấp cứu ghi nhận nhịp nhanh trên thất với khoảng RP kéo dài (hình 1A và hình S1 trong phần phụ lục). Tiêm tĩnh mạch Adenosine, sau 1 nhịp ngoại tâm thu thất và một cơn ngoại tâm thu nhĩ ngắn, nhịp trở về nhịp xoang bình thường. Điều quan trọng cần lưu ý là sự kiện cuối cùng quan sát được khi ngừng nhịp nhanh trên thất của bệnh nhân là phức bộ QRS chứ không phải sóng P, sóng P quan sát trước đó là kích hoạt nhĩ từ cao đến thấp, thấy ở chuyển đạo DII (hình 1B). Điện tâm đồ 12 chuyển đạo sau đó ghi nhận là nhịp nhanh xoang (hình 1C).
Bác sĩ Hills-Evans: mức alkaline phosphatase là 165 U/L (khoảng tham chiếu 27-129); các xét nghiệm chức năng gan khác đều bình thường. Xét nghiệm nước tiểu tìm beta human chorionic gonadotropin thì âm tính.
Tổng phân tích nước tiểu cho thấy tỷ trọng 1.013, ketones 2+ và hồng cầu 2+, cũng như 2 tế bào bạch cầu (giá trị bình thường 0-4). Sàng lọc các độc tố trong nước tiểu ghi nhận dương tính với fentanyl, oxycodon và cannabinoids. Kết quả các xét nghiệm khác xem trong bảng 1. Làm thêm cận lâm sàng hình ảnh học.
Bác sĩ Anderson: Xquang ngực cho thấy phổi trong, bóng tim bình thường, không phù phổi và không có hạch bạch huyết ở trung thất và rốn phổi. CT scan ổ bụng và chậu, có tiêm thuốc cản quang cho thấy sỏi thận 2 bên nhỏ, không gây tắc nghẽn, thận không ứ nước. Trong pha tĩnh mạch cửa, mức đậm độ gan thấp hơn 27 đơn vị Hounsfield so với mức đậm độ lách, hình ảnh phù hợp gan nhiễm mỡ. Không tắc ruột hoặc viêm cấp tính trong vùng bụng và chậu.
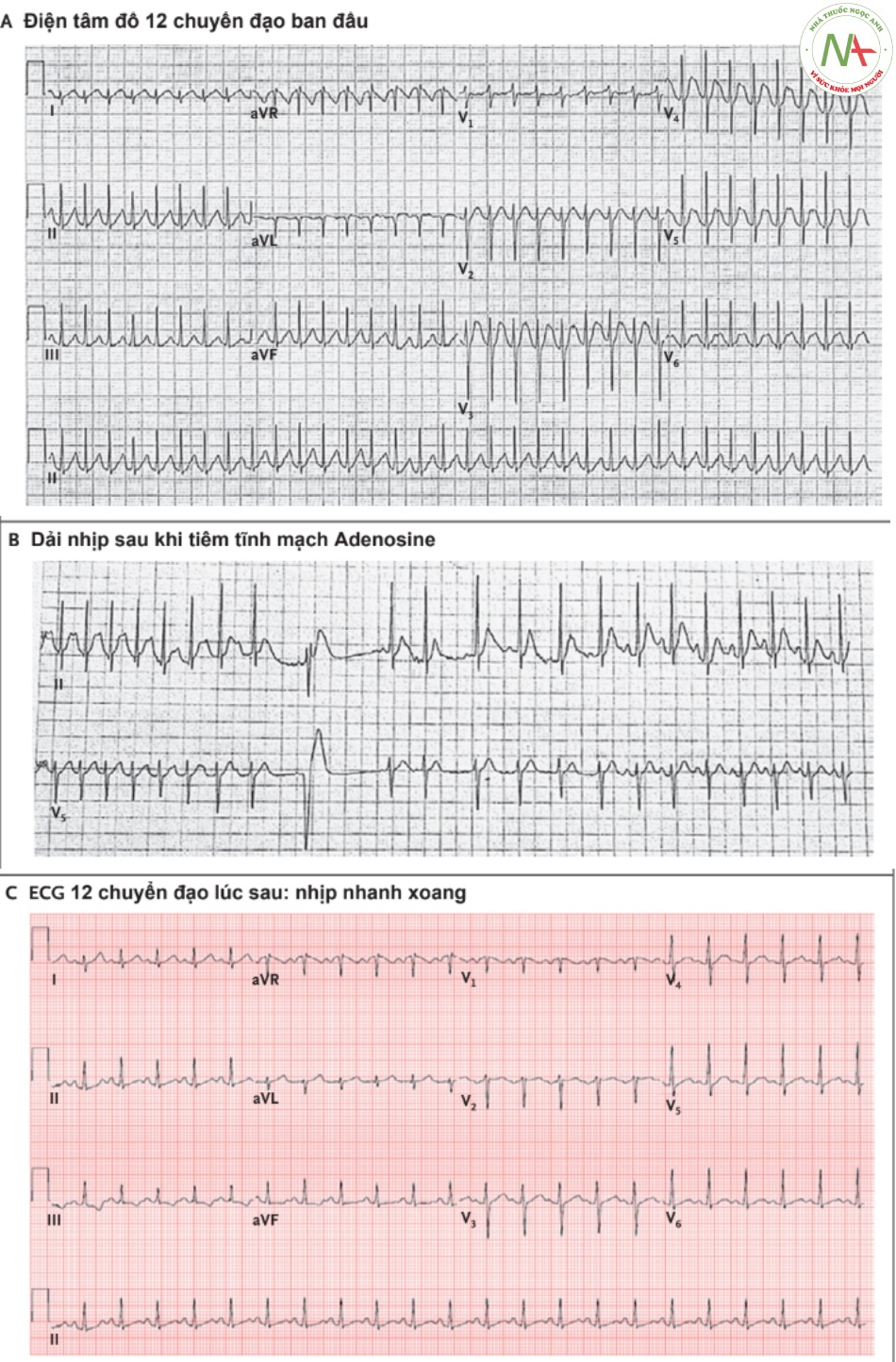
Điện tâm đồ 12 chuyển đạo (hình A) ghi nhận nhịp nhanh trên thất; ECG cũng cho thấy đoạn RP kéo dài (hình S1 trong phần phụ lục). Dải nhịp xoang ghi nhận sau khi dùng Adenosine (hình B) cho thấy đã ngưng nhịp nhanh trên thất. Sau 1 nhịp ngoại tâm thu thất và một cơn ngắn ngoại tâm thu nhĩ, xuất hiện nhịp nhanh xoang. Điện tâm đồ 12 chuyển đạo tiếp theo (hình C) là nhịp nhanh xoang.
Ruột thừa bình thường và các buồng trứng trong giai đoạn tiền mãn kinh, chứa các nang chức năng (hình 2). Bác sĩ Hills-Evans: điều trị bằng dịch truyền tĩnh mạch, ondansetron, pantoprazole, fentanyl và lorazepam. Bệnh nhân chuyển vào phòng bệnh nặng (ICU) và làm các xét nghiệm chẩn đoán.
Xét nghiệm Giá trị tham chiếu Kết quả xét nghiệm cách đây 1 tuần, tại bệnh viện địa phương
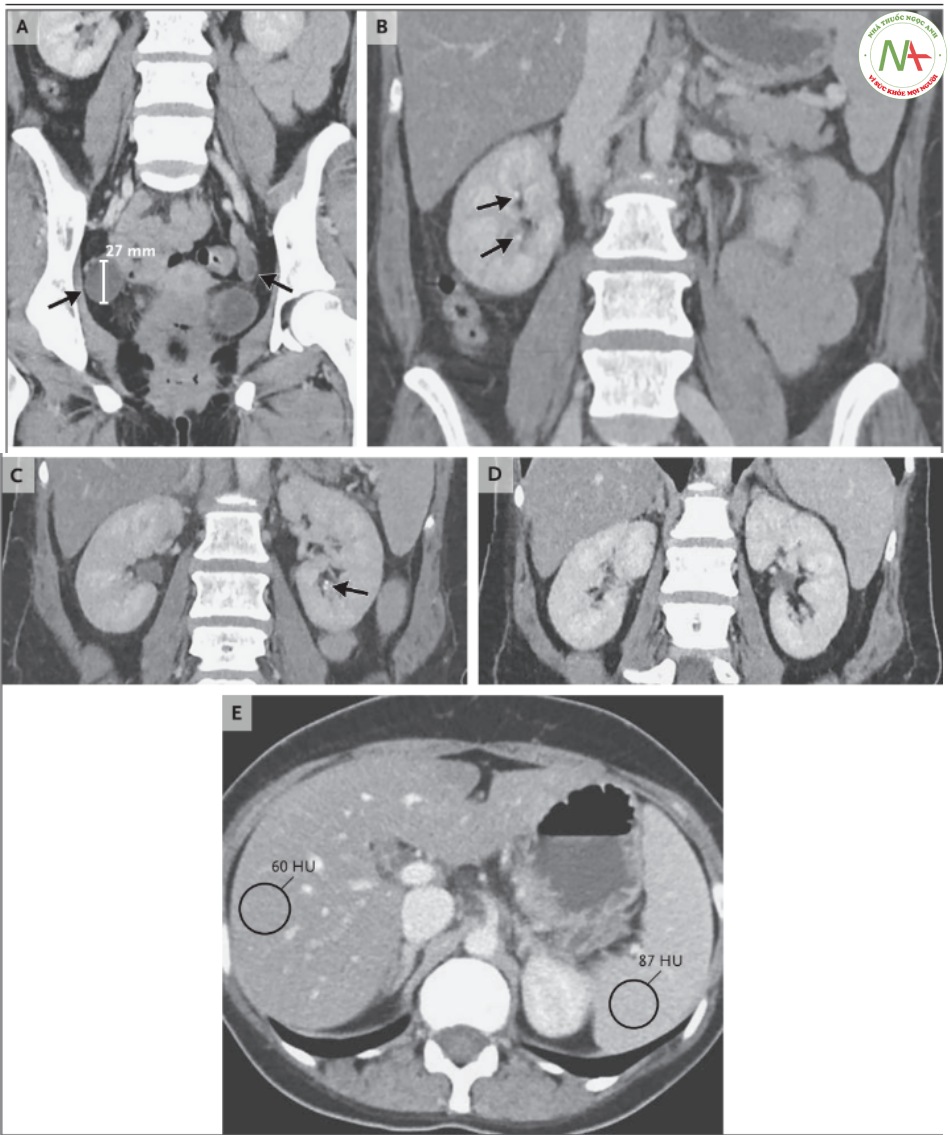
Tiến hành chụp CTscan ổ bụng và chậu sau khi tiêm thuốc cản quang. Hình ảnh tái tạo mặt cắt trước-sau (hình A đến D) cho thấy buồng trứng tiền mãn kinh bình thường chứa các nang chức năng (hình A, mũi tên), cũng như sỏi thận 2 bên, nhỏ, không gây tắc nghẽn (hình B và C, mũi tên) thận không ứ nước (hình D). Mặt cắt trên-dưới (hình E) cho thấy pha tĩnh mạch cửa, đậm độ gan là 27 Hounsfield (HU) thấp hơn đậm độ lách (hình tròn), phù hợp với gan nhiễm mỡ.
Chẩn đoán phân biệt
Bác sĩ Chiappa: Bệnh nhân 39 tuổi này bị nôn nôn ói, đau bụng và kích động có một cơn nhịp nhanh phức bộ QRS hẹp, với tần số tim hơn 200 lần/phút. Bước đầu tiên của tôi để thiết lập chẩn đoán phân biệt là xác định
chính xác loại và nguồn gốc giải phẫu của nhịp nhanh để tìm ra cơ chế gây rối loạn nhịp tim và do đó bệnh cảnh này đang thúc đẩy diễn tiến bệnh. Ngoài ra, để có được chẩn đoán duy nhất, tôi cần xem xét một vài các
triệu chứng khác trong bệnh sử, gồm đau bụng tái phát, sụt cân nhiều chỉ trong 11 tuần và xuất hiện hành vi kỳ quái có đặc trưng là kích động và áp lực phải nói.
Tiếp cận nhịp nhanh trên thất
Dải nhịp trên bệnh nhân cho thấy nhịp tim nhanh với một phức bộ QRS hẹp, bằng chứng phù hợp nhịp nhanh trên thất. Nhịp tim đều không giống bị rung nhĩ hay nhịp nhanh nhĩ đa ổ. Khởi phát đột ngột không giống nhịp nhanh xoang. Trong nhịp nhanh xoang, tôi cho rằng phải có một giai đoạn tăng tốc, chứ không đột ngột tăng lên 200 lần/phút. Tôi nghi ngờ nhịp nhanh trên thất của bệnh nhân này với nhịp tim đều là 1 trong 3 loại; nhịp nhanh vào lại nút nhĩ thất; nhịp nhanh vào lại nhĩ thất, do dẫn truyền ngược dòng qua đường phụ; hoặc nhanh nhĩ đơn ổ.
Phân biệt 3 loại nhịp nhanh trên thất này yêu cầu phải đánh giá sóng P, nhưng tần số thất cao như trên bệnh nhân này, sóng P có thể bị che khuất, chôn vùi bên trong hoặc chồng lên sóng T hoặc phức bộ QRS. Bệnh nhân được điều trị bằng adenosine để làm chậm tần số thất và làm rõ tất cả sóng P cho phép đánh giá tần số, đặc điểm hình thái và vị trí trong chu kỳ tim. Tuy nhiên, sử dụng adenosine cũng chấm dứt nhịp nhanh trên thất, có thể xảy ra trên bệnh nhân nhịp nhanh vào lại nút nhĩ thất, nhịp nhanh vào lại nhĩ thất và một số dạng nhịp nhanh nhĩ. Trước khi chấm dứt nhịp nhanh trên thất, dùng adenosine làm chậm tần số thất và chứng tỏ những gì tôi nghi ngờ là sóng P nằm cuối sóng T, với khoảng RP dài. Tóm lại, tôi nghĩ nhịp nhanh nhĩ là cơ chế có khả năng nhất gây nhịp nhanh trên thất ở bệnh nhân này.
Bất kể cơ chế cụ thể nào, tôi biết bệnh nhân này rất dễ bị nhịp nhanh trên thất. Điều gì gây ra nhịp nhanh trên thất trong trường hợp này?
Các nguyên nhân chính của nhịp nhanh trên thất
Thiếu máu cục bộ, rối loạn điện giải hoặc biến động nhịp tim, trương lực tự động hoặc độ pH của mô khu trú có thể dẫn đến nhịp nhĩ hoặc nhịp thất sớm, do đó có thể gây nhịp nhanh trên thất trên những bệnh nhân nhạy cảm. Thiếu máu cục bộ cơ tim không giống trên bệnh nhân này vì bệnh nhân còn trẻ và không bị đau ngực, không có dấu thiếu máu cơ tim trên điện tâm đồ hoặc tăng troponin. Mặc dù tiền sử có hội chứng nôn ói chu kỳ và gần đây buồn nôn kèm nôn ói, các kết quả cận lâm sàng không cho thấy tăng điện giải đồ có ý nghĩa lâm sàng hoặc bất thường pH máu. Tăng nhịp tim dường như là nguyên nhân gây nhịp nhanh trên thất trên bệnh nhân này. Sinh hiệu ban đầu là dấu hiệu nhịp tim nhanh và sau đó tiêm adenosine, đã điều trị hoàn toàn nhịp nhanh trên thất, điện tim về nhịp nhanh xoang cơ bản.
Các nguyên nhân chính của nhịp nhanh xoang
Các nguyên nhân chính gây nhịp nhanh xoang cần xem xét trên bệnh nhân này gồm đau, nhiễm trùng, chảy máu và giảm thể tích tuần hoàn. Bệnh nhân than phiền đau bụng và sờ đau, nhưng cơn nhịp nhanh dường như
không tương xứng với cơn đau bụng và hình ảnh học cận lâm sàng. Mặc dù đau có thể làm tăng đáng kể nhịp tim trên lâm sàng, nhưng đặc điểm đau mà bệnh nhân mô tả không đến mức gây mức độ nhịp nhanh thất này.
Nhịp nhanh liên quan khởi phát của nhiễm trùng như nhiễm trùng huyết và sốc do thủng ruột hoặc thiếu máu ruột, không có khả năng xảy ra nếu không tụt huyết áp, các dấu hiệu khu trú khi khám lâm sàng, tăng số lượng bạch cầu và sốt kéo dài. Hơn thế nữa, hình Xquang ngực và CTscan ổ bụng không ghi nhận ổ nhiễm trùng và diễn tiến trong ổ bụng không thể giải thích các đặc điểm khác trên lâm sàng của bệnh nhân như kích động, áp lực phải nói và một số hành vi kỳ quái.
Phản ứng bình thường với giảm thể tích tuần hoàn nặng do chảy máu hoặc mất nước là nhịp tim nhanh; tăng nhịp tim để bù trừ và duy trì huyết động. Bệnh nhân này không có tiền sử chảy máu và Hct cao hơn giá trị tham chiếu nên chảy máu cấp tính không phù hợp dẫn đến nhịp nhanh trên bệnh nhân. Giảm thể tích tuần hoàn do nôn ói và mất nước có thể xảy ra, nhưng natri máu và creatinine bình thường, lactate tăng nhẹ chống lại sự hiện
diện tình trạng giảm thể tích máu nặng đủ để gây nhịp nhanh.
Cho đến thời điểm này, tôi đã tập trung xác định nguyên nhân gây nhịp nhanh trên bệnh nhân này. Tuy nhiên, để thu được chẩn đoán chính xác, tôi cần xem xét một vài đặc điểm lâm sàng khác gồm đau bụng, sốt sụt cân và
kích động.
Sỏi thận
Bệnh nhân này có tiền sử sỏi thận. Biểu hiện lâm sàng của bệnh nhân có thể do đường đi của sỏi thận không? Đau liên quan sỏi thận chắc chắn gây đau nặng và dựa vào vị trí của viên sỏi, đôi khi có thể bắt chước cơn đau
bụng cấp tính. Khi một viên sỏi gây tắc nghẽn và thận ứ nước, có thể diễn tiến nhiễm trùng niệu và nôn ói có thể là nguyên nhân nổi bật.
Một vài khía cạnh trong bệnh sử gợi ý chẩn đoán này. Đầu tiên, bệnh nhân có tiền sử sỏi thận, không tắc nghẽn trên hình ảnh CTscan. Thứ hai, bệnh nhân có hồng cầu niệu 2+, có thể do kinh nguyệt, cũng có thể do đường đi
của sỏi thận gây chảy máu. Tuy nhiên, hình ảnh học không cho thấy bằng chứng tắc nghẽn đường niệu; không có thận ứ nước. Do đó, chẩn đoán sỏi thận là nguyên nhân gây nhịp nhanh và các triệu chứng lâm sàng khác thì
không phù hợp.
Dùng chất kích thích
Bệnh nhân có tiền sử dùng nhiều chất kích thích như cocaine, MADA, thuốc phiện và tetrahydrocannabnol. Các triệu chứng nhịp nhanh và kích động trên bệnh nhân có thể phù hợp với tình trạng nhiễm độc cocaine hoặc MDMA, nhưng xét nghiệm sàng lọc độc tố không tìm thấy các chất kích thích này. Ngưng dùng thuốc phiện có thể giải thích nhịp nhanh, kích động, buồn nôn, nôn ói và đau bụng. Tuy nhiên, bệnh nhân không có tiêu chảy, ngáp, nổi da gà hoặc đồng tử giãn 2 bên, những biểu hiện phù hợp hội chứng cai thuốc phiện. Xét nghiệm độc tố dương tính với fetanyl và cannabinoids, một trong 2 chất này có thể lẫn với 1 chất không xác định mà không thể phát hiện bằng các phương pháp xét nghiệm độc chất hiện nay. Mặc dù tôi không thể loại trừ khả năng nhiễm độc hoặc hội chứng cai thuốc gây nhịp nhanh, tôi muốn tránh tập trung vào tiền sử chất gây nghiện để tránh thu hẹp sớm chẩn đoán phân biệt.
Hội chứng Serotonin
Serotonin là một cân nhắc quan trọng trên bệnh nhân này vì than phiền sốt ở nhà, run giật và kích động. Thuốc phiện, ondansetron, MDMA và cocaine tất cả đều liên quan hội chứng này. Tuy nhiên, thậm chí nếu tôi cho rằng bệnh nhân đã dùng một thuốc kích thích serotonergic, theo tiêu chuẩn Hunter (một quy tắc quyết định hỗ trợ chẩn đoán hội chứng serotonin), bệnh nhân không có tăng phản xạ và rung giật sẽ loại trừ hội chứng serotonin.
U quái buồng trứng
Mặc dù bệnh nhân tỉnh và định hướng tốt, nói nhanh và áp lực phải nói cùng với cảm xúc không ổn định. Bệnh nhân sụt khoảng 7kg kể từ lần nhập viện đầu tiên, trong 11 tuần trước lần nhập viện này. Kết hợp sụt cân, đau bụng và thay đổi hành vi trên bệnh nhân nữ 39 tuổi làm dấy nên mối lo ngại ung thư, có thể là u quái buồng trứng do viêm não rìa. Tuy nhiên, chẩn đoán này sẽ không thể giải thích nhịp nhanh và mặc dù bệnh nhân có tiền sử nang buồng trứng, hình ảnh học đã loại trừ u quái buồng trứng hoặc khối tổn thương khác trên buồng trứng.
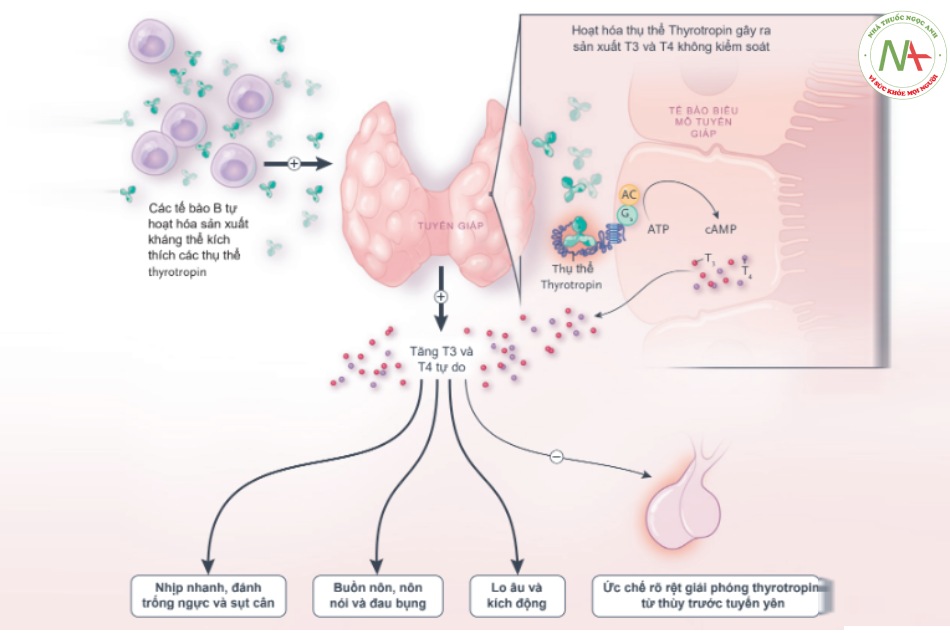
Cường giáp
Sự kết hợp nhịp nhanh và sụt cân, 2 biểu hiện lâm sàng quan trọng nhất trong bệnh sử gợi ý cường giáp. Khi tôi xem xét sụt cân và nhịp nhanh trong bối cảnh bệnh nhân kích động, nôn ói và các dấu hiệu tâm-thần kinh như cảm xúc không ổn định, ánh nhìn dữ tợn, áp lực phải nói, run nhẹ, ban đỏ và da ấm – chẩn đoán cường giáp tăng lên hàng đầu trong chẩn đoán phân biệt của tôi. Hơn thế nữa, nhịp nhanh trên thất được kích thích trên cơ sở nhịp nhanh xuất hiện trong bệnh cảnh nhiễm độc giáp sẽ thành lập một
chẩn đoán thống nhất trên ca này. Ở các vùng địa lý, những bệnh nhân ăn đủ iod, cường giáp thường do bệnh Graves hoặc bệnh tuyến giáp dạng nốt. Để đưa ra chẩn đoán, tôi sẽ làm xét nghiệm chức năng tuyến giáp cũng như xét nghiệm tự kháng thể trong bệnh tuyến giáp tự miễn. Nếu các xét nghiệm vẫn không chẩn đoán bệnh Graves, làm thêm các nghiên cứu để tìm nguyên nhân khác – các nguyên nhân ít có khả năng gây cường giáp khác.
Chẩn đoán của bác sĩ Victor Chiappa
Cường giáp
Thảo luận bệnh học trên ca lâm sàng
Bác sĩ Melis N. Anahtar: làm các xét nghiệm chức năng tuyến giáp. Nồng độ thyrotropin trong máu không thể phát hiện được, thyroxine tự do (T4) và triiodothyronine total (T3) đều cao hơn mức giới hạn trên; những kết quả này phù hợp với chẩn đoán cường giáp nặng. Để đánh giá bệnh tuyến giáp tự miễn, làm xét nghiệm các kháng thể thyroide peroxidase và các thụ thể thyrotropin. Nồng độ kháng thể thyroide peroxidase bình thường và thụ thể thyrotropin là 29 U/L (khoảng tham chiếu 0-1.75). Xét nghiệm kháng thể thụ thể thyrotropin, phát hiện bất kỳ kháng thể nào liên kết trong vùng thụ thể thyrotropin, có độ nhạy và độ đặc hiệu khoảng 97% đối với bệnh Graves chưa điều trị.
Ngoài làm thêm xét nghiệm để xác định cụ thể sự hiện diện của globulin miễn dịch kích thích tuyến giáp (TSI), một loại kháng thể thụ thể thyrotropin mà kích hoạt trực tiếp tín hiệu của thụ thể thyrotropin và được cho là nguyên nhân gây ra các dấu hiệu lâm sàng trong bệnh Graves (hình 3). TSI được đo bằng xét nghiệm sinh học nhạy cảm sử dụng dòng tế bào đã được xử lý công nghệ biểu hiện thụ thể thyrotropin ở người và gen luciferase reporter tạo ra một monophosphate adenosine vòng. Chỉ số TSI cao hơn 1.8 (khoảng tham chiếu <1.3) có độ nhạy và độ đặc hiệu gần như 100% trong bệnh Graves chưa điều trị. Chỉ số TSI trên bệnh nhân này là 7.5, nên chẩn đoán xác định bệnh Graves.
Mức độ tăng của chỉ số TSI này liên quan đến kém đáp ứng điều trị với các thuốc kháng giáp, tăng nguy cơ nhiễm độc giáp thai nhi nếu bệnh nhân mang thai và tăng nguy cơ mắc bệnh về mắt do bệnh Graves.
Bác sĩ Anderson: ngoài các xét nghiệm đặc hiệu tuyến giáp, nên làm thêm siêu âm tuyến giáp để phân biệt viêm giáp lan tỏa với một nốt tăng chức năng hoặc bệnh phình giáp đa nốt. Trên hình ảnh siêu âm doppler màu, thang xám của tuyến giáp nằm dọc và ngang, kích thước dọc nằm ở mặt phẳng ngang trên giới hạn bình thường và kết cấu phản âm nhu mô không đồng nhất nhẹ (hình 4). Trên hình ảnh Doppler màu, có sự sung huyết rõ rệt trong toàn bộ tuyến giáp, một đặc trưng trong bệnh Graves và được gọi là “ dấu địa ngục”. Dạng dòng chảy doppler này cho thấy độ nhạy cao (88-95%) và độ đặc hiệu cao (95%) trong bệnh Graves, và tốc độ đỉnh tâm thu cao hơn trên bệnh nhân mắc bệnh Graves hơn là ở bệnh nhân viêm giáp do các nguyên nhân khác. Các cấu trúc không phải tuyến giáp nằm sát nhau
không cho thấy dòng doppler ngẫu nhiên hoặc nhân tạo. Sự không đồng nhất và kích thước của tuyến giáp không phải các bằng chứng đặc hiệu nhưng nên xem xét trong chẩn đoán bệnh Graves.
Thảo luận Điều trị
Bác sĩ Nikolaos Stathatos: Bệnh nhân này phù hợp với tiêu chuẩn ngộ độc giáp nặng (cơn bão giáp), một chẩn đoán liên quan tỷ lệ tử vong lên đến 30%. Vì mức độ nặng của biểu hiện lâm sàng thần kinh, tim mạch và tiêu hóa, bệnh nhân được chuyển vào ICU để điều trị tích cực hơn. Ngoài điều trị hỗ trợ bằng các thuốc chẹn beta và dịch truyền, bệnh nhân được điều trị ban đầu bằng propylthiouracil, chuyển sang methimazole trong vòng 24h. Bệnh nhân đáp ứng nhanh với điều trị, cải thiện triệu chứng lâm sàng và kết quả xét nghiệm chức năng tuyến giáp trong 4-5 ngày đầu.
Đáp ứng nhanh với điều trị của bệnh nhân có thể liên quan không chỉ đưa ra chẩn đoán cường giáp và tiến hành điều trị ban đầu các thuốc kháng giáp mà còn dùng thuốc cản quang iod trong CT bụng. Lượng lớn iod có thể gây hiệu ứng Wolff-Chaikoff (giảm sản xuất hormone giáp do uống 1 lượng lớn iod như cho bệnh nhân nhân iod trong các nghiên cứu hình ảnh học) trong tuyến giáp của bệnh nhân, dẫn đến tình trạng ngừng hoạt động cấp tính của tuyến giáp.

Sau đó, các thuốc kháng giáp ban đầu giúp kiểm soát lâu dài cường giáp. Ngược lại, 11 tuần trước nhập viện lần này, bệnh nhân khởi phát các triệu chứng tương tự có thể liên quan cường giáp không được chẩn đoán, bệnh nhân hấp thụ 1 lượng lớn chất cản quang thông qua chụp CT bụng có cản quang, có thể gây ra các ảnh hưởng tương tự. Tuy nhiên, Bệnh nhân không dùng thuốc kháng giáp sau khi nhập viện, tuyến giáp của bệnh nhân có thể “thoát khỏi” tác dụng ức chế ngắn hạn của lượng iod và cường giáp lại tái phát nặng hơn, dẫn đến tình trạng hiện tại và phải nhập viện.
Diễn tiến bệnh phòng, bệnh nhân đáp ứng tốt với điều trị và xuất viện về nhà; bệnh nhân đến tái khám bác sĩ nội tiết. Tuy nhiên, kết quả xét nghiệm chức năng tuyến giáp được làm vài tháng sau cho thấy kém tuân thủ điều trị, với tăng T3 và T4. Bệnh nhân sau đó không còn theo dõi điều trị.
Bác sĩ lâm sàng: Loại nhịp nhanh trên thất nào mà bác sĩ điều trị nghĩ bệnh nhân mắc phải?
Bác sĩ Barrett: Nhịp nhanh nhĩ có khả năng nhất. Các đặc điểm hình thái và thời gian sóng P không phù hợp nhịp nhanh vào lại nút nhĩ thất. Mặc dù có thể dừng nhịp nhanh trên thất bằng đường phụ với adenosine, nhưng nhiều khả năng nhịp nhanh trên thất trên bệnh nhân này là nhịp nhanh nhĩ nhạy cảm adenosine.
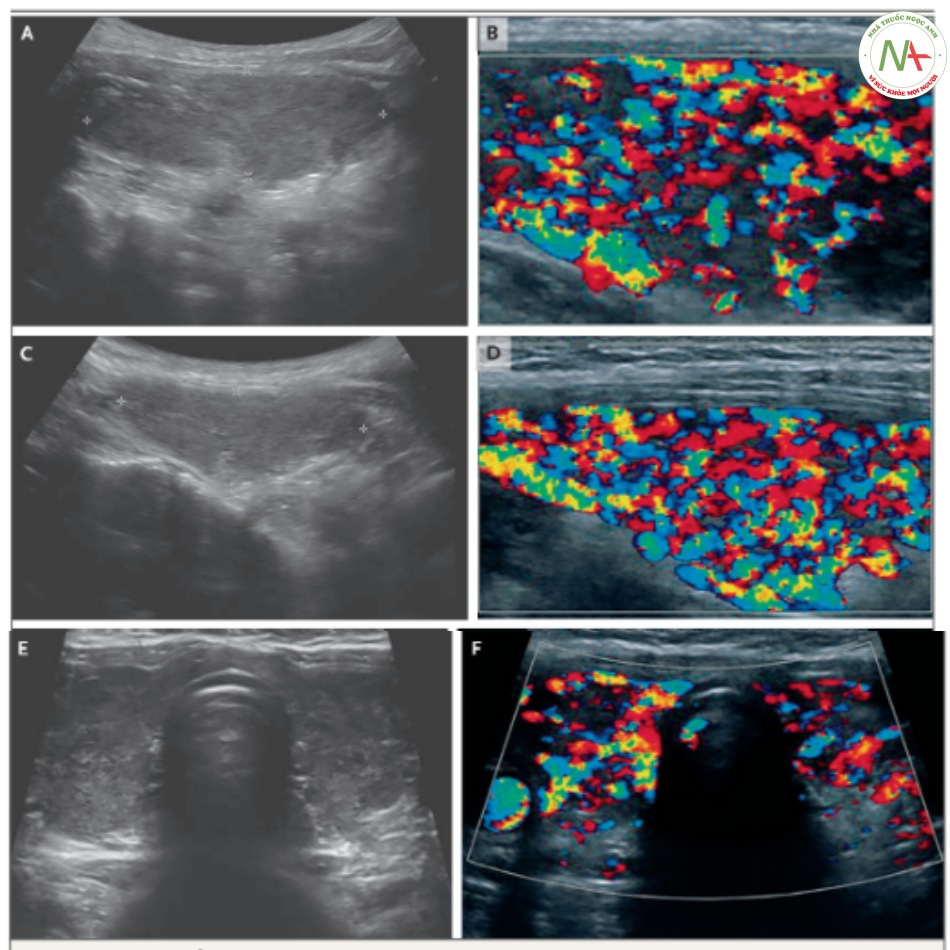
Trên thang xám hình ảnh dọc giữa (hình A và C) và thang xám hình ảnh ngang (hình E), kích thước nằm ở giới hạn trên mức bình thường và kết cấu phản âm nhu mô không đồng nhất nhẹ. Trên hình doppler màu tương ứng (hình B, D và F), có hiện tượng sung huyết rõ rệt toàn bộ tuyến giáp, là nột đặc trưng của bệnh Graves và được gọi là “dấu địa ngục” (inferno sign). Các cấu trúc khôn phải tuyến giáp nằm sát nhau cho thấy không có dòng doppler ngẫu nhiên hoặc nhân tạo.
Trong một cơn nhịp nhanh nhĩ như vậy, adenosine chấm dứt nhịp tim nhanh trong nhịp nhanh nhĩ; nhịp quan sát được cuối cùng dẫn đến tâm thất, tạo ra phức bộ QR không có hoạt động ngoại tâm nhĩ đơn ổn, là nguyên nhân gây nhịp nhanh trên thất.
Bác sĩ lâm sàng: Bệnh nhân có được điều trị bằng glucocorticoids khi mắc cơn bão giáp không?
Bác sĩ Stathatos: Mặc dù glucocorticoids giảm chuyển hóa T4 thành T3 ở ngoại biên và có thể được dùng để điều trị cơn bão giáp, glucocorticoids không được dùng trên bệnh nhân này vì bệnh nhân có huyết động không ổn định và đáp ứng nhanh với điều trị bằng propylthiouracil.
Bác sĩ lâm sàng: Bạn có nghĩ không có quan hệ giữa tiền sử sỏi thận của bệnh nhân và chẩn đoán cường giáp?
Bác sĩ Stathatos: Cường giáp là nguyên nhân hàng đầu tăng canci máu. Điều này đặc biệt liên quan trên bệnh nhân cường giáp nặng về mặt sinh hóa. Tuy nhiên, bệnh nhân này không bao giờ tăng canxi máu từ lúc nhập viện. Không có mối liên hệ giữa sỏi thận và cường giáp ngay cả trong bệnh cảnh tăng canxi máu do cường giáp.
Chẩn đoán sau cùng
Cường giáp do bệnh Graves.
References
1. Iqbal MM, Basil MJ, Kaplan J, Iqbal MT. Overview of serotonin syndrome. Ann Clin Psychiatry 2012; 24: 310-8.
2. Dunkley EJ, Isbister GK, Sibbritt D, Dawson AH, Whyte IM. The Hunter Sero-tonin Toxicity Criteria: simple and accu-rate diagnostic decision rules for serotonin toxicity. QJM 2003; 96: 635-42.
3. Klein I, Danzi S. Thyroid disease and the heart. Circulation 2007; 116: 1725-35.
4. Wustmann K, Kucera JP, Zanchi A, et al. Activation of electrical triggers of
atrial fibrillation in hyperthyroidism.J Clin Endocrinol Metab 2008; 93: 2104-8.
5. Nordyke RA, Gilbert FI Jr, Harada AS. Graves’ disease: influence of age on clini-cal findings. Arch Intern Med 1988; 148:626-31.
6. Rosenthal FD, Jones C, Lewis SI. Thy-rotoxic vomiting. Br Med J 1976; 2: 209-11.
7. Stern RA, Robinson B, Thorner AR, Arruda JE, Prohaska ML, Prange AJ Jr. A sur-vey study of neuropsychiatric complaints in patients with Graves’ disease. J Neuropsy-chiatry Clin Neurosci 1996; 8: 181-5.
8. Schott M, Hermsen D, Broecker-Preuss M, et al. Clinical value of the first auto-mated TSH receptor autoantibody assay for the diagnosis of Graves’ disease (GD):an international multicentre trial. Clin En-docrinol (Oxf) 2009; 71: 566-73.
9. Thyretain TSI Reporter BioAssay. Athens, OH: Diagnostic HYBRIDS, 2009
(package insert).
10. Barbesino G, Tomer Y. Clinical utility of TSH receptor antibodies. J Clin Endo-crinol Metab 2013; 98: 2247-55.
11. Ralls PW, Mayekawa DS, Lee KP, et al. Color-flow Doppler sonography in Graves disease: “thyroid inferno.” AJR Am J Roentgenol 1988; 150: 781-4.
12. Aldasouqi S, Sheikh A, Klosterman P. Doppler ultrasonography in the diagnosis of Graves disease: a non-invasive, widely under-utilized diagnostic tool. Ann Saudi Med 2009; 29: 323-4.
13. Arslan H, Unal O, Algün E, Harman M, Sakarya ME. Power Doppler sonogra-phy in the diagnosis of Graves’ disease. Eur J Ultrasound 2000; 11: 117-22.
14. Cappelli C, Pirola I, De Martino E, et al. The role of imaging in Graves’ dis-ease: a cost-effectiveness analysis. Eur J Radiol 2008; 65: 99-103.
15. Chaudhary V, Bano S. Thyroid ultra-sound. Indian J Endocrinol Metab 2013; 17: 219-27.
16. Saleh A, Cohnen M, Fürst G, Gode-hardt E, Mödder U, Feldkamp J. Differen-tial diagnosis of hyperthyroidism: Doppler sonographic quantification of thyroid blood flow distinguishes between Graves’disease and diffuse toxic goiter. Exp Clin Endocrinol Diabetes 2002; 110: 32-6.
17. Burch HB, Wartofsky L. Life-threaten-ing thyrotoxicosis: thyroid storm. Endocri-nol Metab Clin North Am 1993; 22: 263-77.
18. Markou K, Georgopoulos N, Kyriazo-poulou V, Vagenakis AG. Iodine-induced hypothyroidism. Thyroid 2001; 11: 501-10.
Để lại một phản hồi