
Nội dung chính
Aminosid (hay Aminoglycosid) là một nhóm kháng sinh tự nhiên hoặc bán tổng hợp có nguồn gốc từ xạ khuẩn. Ban đầu nó được sử dụng rộng rãi như là một nhóm kháng sinh hàng đầu trong điều trị nhiễm trùng, nhưng từ những năm 1980 nó đã dần bị thay thế bởi Cephalosporin, Carbapenem và Quinolon.
Lịch sử nghiên cứu và phát triển
Kháng sinh đầu tiên trong nhóm này được phát hiện bởi Waksman là streptomycin, được phân lập từ Streptomyces griseus, được đưa vào sử dụng lâm sàng từ năm 1944. Tiếp theo lần lượt các kháng sinh khác trong nhóm cũng được giới thiệu: neomycin, 1949, từ S.fradiae; kanamycin, 1957, từ S.kanamyceticus; gentamicin, 1963, từ Micromonospora purpurea; netilmicin, 1967, bán tổng hợp từ sisomicin của M.inyonensis; tobramycin, 1967, từ S.tenebrarius. Sau đó từ những năm 1980 nó đã dần bị thay thế bởi Cephalosporin thế hệ 3, Carbapenem và Quinolon, do các thuốc này được coi là ít độc hơn, và có phổ kháng khuẩn rộng hơn. Tuy nhiên việc gia tăng sự đề kháng với các nhóm kháng sinh này, kết hợp với các kiến thức sâu rộng hơn về Aminosid, người ta bắt đầu quan tâm phát triển các Aminosid mới, như arbekacin và plazomicin. Các Aminosid sau này được thiết kế để chống lại các cơ chế đề kháng phổ biến, do đó duy trì khả năng chống lại các mầm bệnh đa kháng thuốc.
Phân loại
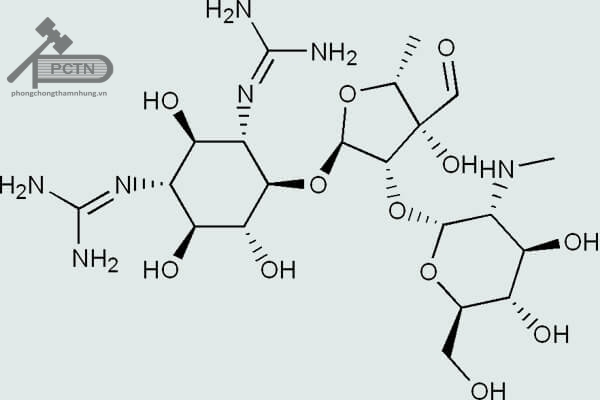
Các Aminosid có cấu trúc chung là Đường-O-Genin. Trong đó, phần đường có thể là đường 5 hoặc 6 cạnh, thường mang nhóm amin. Phần genin có thể mang cấu trúc 1,3-diaminocyclitol hoặc 1,4-diaminocyclitol. Tuy nhiên chúng ta sẽ không đi sâu vào cấu trúc từng nhóm phân loại. Có thể phân loại đơn giản theo nguồn gốc có Aminosid thiên nhiên và Aminosid bán tổng hợp.
Bảng phân loại (mang tính tham khảo) dưới đây có thể giúp bạn đọc có cái nhìn chi tiết hơn:
|
Dẫn chất 1,3-diaminocyclitol |
Dẫn chất 1,4-diaminocyclitol |
|||||
|
Genin |
Streptamin |
Streptidin |
Deoxy-2-streptamin |
Fortamin |
||
|
Thiên nhiên |
Spectinomycin |
Streptomycin |
Thế 4,5 |
Thế 4,6 |
Thế 4 |
Fortimicin A |
|
Neomycin Framycetin Paromomycin Lividomycin Ribostamycin Butirosin |
Kanamycin Gentamicin Tobramycin Sisomicin |
Apramycin |
||||
|
Bán tổng hợp |
|
Dihydrostrep-tomycin |
|
Dibekacin Netilmicin |
|
|
Phổ kháng khuẩn
Aminosid là nhóm kháng sinh có phổ tác dụng đặc trưng trên hầu hết vi khuẩn gram(-), một số chọn lọc trên cả các chủng vi khuẩn gram(+). Tuy vậy mỗi kháng sinh có hoạt tính nổi trội trên một hoặc một số chủng vi khuẩn nhất định, ví dụ:
Streptomycin: nhạy cảm với các Mycobacterium (lao, phong), kanamycin cũng nhạy cảm trên các vi khuẩn này nhưng yếu hơn streptomycin.
Gentamicin: nhạy cảm với nhiều vi khuẩn gram(-) và gram(+), đặc biệt trên MRSA, P.aeruginosa. Tobramycin có hoạt lực trên P.aeruginosa cao hơn gentamicin.
Paramomycin: tác dụng trên kí sinh trùng (amip, sán ruột).
Spectinomycin: nhạy cảm đặc biệt với N.gonorrhoeae (lậu cầu).
Một điều quan trọng để các Aminosid phát huy tác dụng đó là nồng độ kháng sinh nội bào phải cao hơn nhiều ở ngoại bào, đó là lí do vì sao chúng có tác dụng kém trên các vi khuẩn kị khí, vì các vi khuẩn này không có cơ chế vận chuyển tích cực các Aminosid.
Cơ chế tác dụng
Aminosid là nhóm kháng sinh diệt khuẩn. Tuy nhiên, dù đã được phát hiện và nghiên cứu từ lâu, các nhà khoa học vẫn chưa thể lí giải được trọn vẹn tác dụng diệt khuẩn của nhóm kháng sinh này. Nhóm Tetracyclin có cơ chế chung là gắn vào tiểu phần 30S của ribosom (gắn có phục hồi) làm ngăn chặn quá trình tổng hợp protein của vi khuẩn, nên nó là kháng sinh kìm khuẩn. Các Aminosid cũng ức chế tổng hợp protein vi khuẩn bằng cách gắn vào tiểu phần 30S của ribosom vi khuẩn và ức chế tổng hợp protein của vi khuẩn. Mặc dù sự gắn này là không hồi phục, nhưng nó cũng chưa đủ để lí giải tác dụng diệt khuẩn của Aminosid.
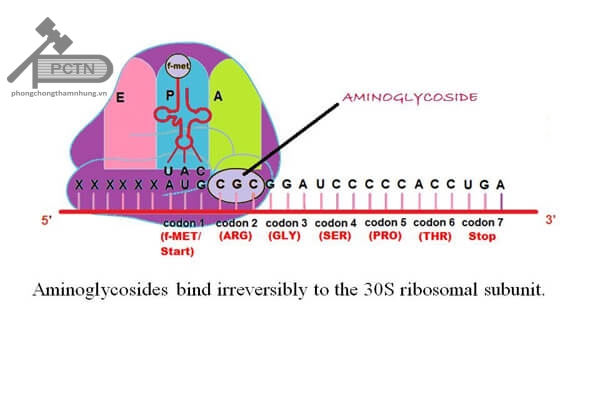
Cần chú ý thêm là với các Aminosid, nồng độ càng cao thì khả năng diệt khuẩn càng tốt (khả năng diệt khuẩn phụ thuộc nồng độ), đồng thời có khả năng ức chế sự phát triển của vi khuẩn nhiều giờ sau khi không còn phát hiện nồng độ Aminosid (tác dụng hậu kháng sinh kéo dài).
Tác dụng
Sử dụng chủ yếu trong các nhiễm trùng gram(-), đặc biệt amikacin hay được sử dụng trong các trường hợp nhiễm trùng nặng và đa kháng.
Tùy theo đặc điểm từng thuốc mà có chỉ định phù hợp:
Streptomycin: dùng trong phác đồ phối hợp điều trị lao.
Gentamicin: nhiễm khuẩn đã kháng β-lactam, điều tri và phòng ngừa nhiễm
P.aeruginosa; nhiễm khuẩn hô hấp, tiết niệu do gram(-).
Neomycin: phối hợp với polymycin B làm thuốc bôi ngoài da; dùng trong trường hợp hôn mê gan khi muốn diệt hệ khuẩn chí đường ruột.
Paramomycin: điều trị lỵ amip và một số kí sinh trùng khác.
Spectinomycin: điều trị lậu (tiêm bắp sâu).
Amikacin: điều trị nhiễm P.aeruginosa, Staphylococcus kháng penicillin; dùng điều trị lao khi streptomycin đã bị kháng; thường dùng amikacin như một kháng sinh thay thế khi các kháng sinh cùng tác dụng khác đã bị kháng.
Tác dụng phụ
Độc với thận: Aminosid được tái hấp thu bởi hiện tượng thẩm bào trong các tế bào lót ở ống lượn gần, tập trung trong các lysosom. Do không có cơ chế đào thải phức hợp aminosid-lysosom nội bào, tế bào trương lên và vỡ ra.
Độc với thính giác khi dùng kéo dài do tác dụng trên dây thần kinh VIII (không hồi phục).
Ức chế dẫn truyền thần kinh cơ: run chân tay…
Cơ chế kháng thuốc của vi khuẩn
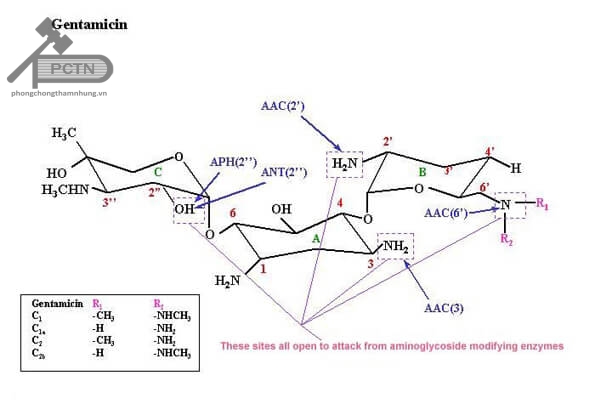
Có 3 cơ chế đề kháng aminosid: giảm tính thấm của màng tế bào với thuốc, đột biến thay đổi đích tác dụng của aminosid hoặc sản xuất các enzym phá hủy thuốc.
- Giảm tính thấm màng tế bào: một số chủng P.aeruginosa và một số vi khuẩn gram(-) khác có khiếm khuyết trong vận chuyển phân tử thuốc qua màng hoặc không cho thuốc thấm qua màng. Cơ chế này có thể truyền qua trung gian nhiễm sắc thể và dẫn đến phản ứng kháng chéo với tất cả các aminosid khác.
- Thay đổi cấu trúc đích tác dụng: đột biến gen quy định vị trí mà aminosid gắn với tiểu phần 30S của ribosom dẫn đến giảm ái lực của aminosid với đích tác dụng, vi khuẩn không bị ức chế tổng hợp protein. Kháng với streptomycin có thể xảy ra theo cơ chế này vì thuốc chỉ gắn vào một vị trí trên tiểu phần 30S. Kháng với các aminosid khác theo cơ chế này là không phổ biến vì các thuốc này gắn vào nhiều vị trí trên tiểu phần 30S, vi khuẩn muốn kháng thuốc theo cơ chế này phải đột biến nhiều lần hơn.
- Sản xuất enzym phá hủy thuốc: đây là cơ chế kháng thuốc phổ biến nhất. Các gen mã hóa cho các enzym này thường được tìm thấy trên plasmid. Trong các trực khuẩn gram(-) việc sản xuất enzym hấu hết là do nhiều gen quy định. Các nhà khoa học giả thuyết rằng các enzyme này có nguồn gốc từ các sinh vật tạo ra aminosid hoặc từ sự đột biến các gen mã hóa cho các enzym liên quan đến hô hấp tế bào. Ba loại enzym phá hủy aminosid là :
N-Acetyltransferase (AAC): acetyl hóa nhóm amin.
O-Adenyltransferase (ANT): adenyl hóa nhóm hydroxyl.
O-Phosphotransferase (APH): phosphoryl hóa nhóm hydroxyl.
Tương tác thuốc

β-lactam (penicillin, cephalosporin): tạo thành cặp phối hợp kháng sinh kinh điển, tạo ra tác dụng hiệp đồng, tăng hiệu quả điều trị, giảm nguy cơ kháng thuốc.
Tìm hiểu thêm về tác dụng hiệp đồng tại: Tương tác thuốc
Thuốc lợi tiểu (furosemid, mannitol): tăng nguy cơ gặp tác dụng phụ trên thận và các tác dụng phụ khác của aminosid do gây tăng nồng độ aminosid huyết thanh và mô.
Thuốc giãn cơ (pancuronium, vecuronium): Các Aminoside can thiệp vào quá trình dẫn truyền Calci gây ức chế sự phóng thích acetylcholin tại tại nút truyền tín hiệu thần kinh – cơ, đồng thời làm giảm độ nhạy cảm của màng sau synap gây tăng nguy cơ suy hô hấp nặng và kéo dài.
Thuốc kháng virus (tenofovir, adefovir): tăng nguy cơ và mức độ độc trên thận.
Kháng sinh Polypeptid (vancomycin, dalbavancin, oritavancin): có nguy cơ gây nhiễm độc thần kinh, liệt hô hấp, tăng độc tính trên thận.
Amphotericin B: gây tăng độc tính trên thận.
Thuốc chống viêm không steroid (NSAIDs): tăng độc tính trên thận.
Thuốc chống đông máu: tăng thời gian prothrombin.
Glucocorticoid: dùng kéo dài có nguy cơ bội nhiễm nấm.
Có thể bạn quan tâm:
Nguyên tắc phối hợp kháng sinh
Để lại một phản hồi